
|
 |
Cathepsin: CTS
[別名]
キーワード
タンパク質分解酵素、リソゾーム
歴史とあらまし
古代ギリシャ語の”消化”に由来し、”down”を表す”kata-“と”boil”を表す”hepsein”を合わせてカテプシンと名付けられた。リソゾームに局在する酸性プロテアーゼの総称で、高等動物のほぼすべての組織、植物、原生動物にも広く存在する。現在までのところ、カテプシンファミリーに属する15種類のプロテアーゼが知られており、活性部位や基質特異性の違いで分類されている(表)。
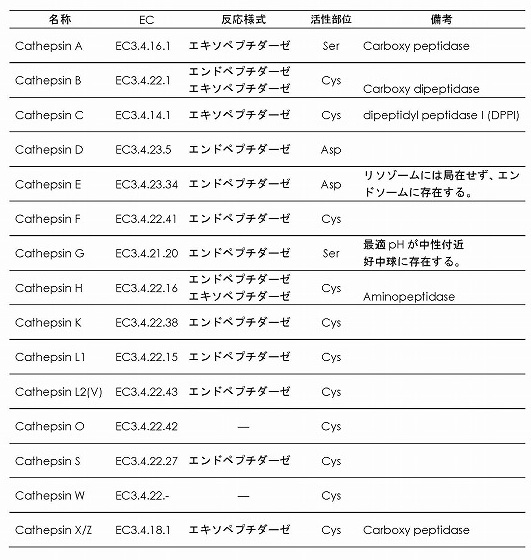 表
表
分子構造
カテプシンファミリーの中で最も多いシステインプロテアーゼは、ジスルフィド結合で結合したheavy chainとlight
chainからなる。テトラマーを形成するカテプシンC以外は、分子量30kDaくらいまでのモノマーとして存在する。
アスパラギン酸プロテアーゼであるカテプシンDもジスルフィド結合で結合したheavy chainとlight
chainからなる。カテプシンEは、ジスルフィド結合したホモダイマーを形成している。これらは、N結合型糖鎖をもつ糖タンパク質である。
機能
カテプシンファミリーはタンパク質分解酵素であるが、その反応様式は様々である(表)。大きく分けて、ペプチド鎖内部のペプチド結合に作用するエンドペプチダーゼと、ペプチド末端に作用するエキソペプチダーゼに分類されるが、その両方の活性を持つカテプシンBやHのようなものもある(Ref. 1,2)。
老化・老年病における意義
アルツハイマー病(Ref. 3,4)や筋ジストロフィー(Ref. 5)、自然老化(Ref. 6,7,8)においてカテプシンDが増加するという報告がある。また、老齢ラットの脳組織のプロテオーム解析よりカテプシンDが老化に伴って細胞質に蓄積することも明らかになっている(Ref. 9)。カテプシンDが細胞質に蓄積する生理的意味は明らかではないが、酸化ストレスやプロテアソームの活性低下が関与している可能性も示唆されている(Ref. 10)。
Database
CTSA, CTSB, CTSC, CTSD, CTSE, CTSF, CTSG, CTSH, CTSK, CTSL1, CTSL2, CTSO, CTSS, CTSW, CTSZ
参考文献
1)Gocheva, V., Joyce, J. A. Cysteine cathepsins and the cutting edge of
cancer invasion. Cell Cycle 6:60-64, 2007 (PMID: 17245112)
2)Turk, V.,
Turk, B., Turk, D. Lysosomal cysteine proteases: facts and opportunities.
EMBO J 20:4629-4633, 2001 (PMID: 11532926)
3)Adamec, E., Mohan, P. S.,
Cataldo, A. M., Vonsattel, J. P., Nixon, R. A. Up-regulation of the
lysosomal system in experimental models of neuronal injury: implications for
Alzheimer's disease. Neuroscience 100:663-675, 2000 (PMID: 11098128)
4)Nakanishi, H., Amano, T., Sastradipura, D. F., Yoshimine, Y., Tsukuba, T.,
Tanabe, K., Hirotsu, I., Ohono, T., Yamamoto, K. Increased expression of
cathepsins E and D in neurons of the aged rat brain and their colocalization
with lipofuscin and carboxy-terminal fragments of Alzheimer amyloid
precursor protein. J Neurochem 68:739-749, 1997 (PMID: 9003065)
5)Gopalan,
P., Dufresne, M. J., Warner, A. H. Thiol protease and cathepsin D activities
in selected tissues and cultured cells from normal and dystrophic mice. Can
J Physiol Pharmacol 65:124-129, 1987 (PMID: 3552162)
6)Kenessey, A.,
Banay-Schwartz, M., DeGuzman, T., Lajtha, A. Increase in cathepsin D
activity in rat brain in aging. J Neurosci Res 23:454-456, 1989 (PMID:
2769800)
7)Nakamura, Y., Takeda, M., Suzuki, H., Morita, H., Tada, K.,
Hariguchi, S., Nishimura, T. Age-dependent change in activities of lysosomal
enzymes in rat brain. Mech Ageing Dev 50:215-225, 1989 (PMID: 2630833)
8)Nakanishi, H., Tominaga, K., Amano, T., Hirotsu, I., Inoue, T., Yamamoto,
K. Age-related changes in activities and localizations of cathepsins D, E,
B, and L in the rat brain tissues. Exp Neurol 126:119-128, 1994 (PMID:
8157122)
9)Sato, Y., Suzuki, Y., Ito, E., Shimazaki, S., Ishida, M.,
Yamamoto, T., Yamamoto, H., Toda, T., Suzuki, M., Suzuki, A., Endo, T.
Identification and characterization of an increased glycoprotein in aging:
age-associated translocation of cathepsin D. Mech Ageing Dev 127:771-778,
2006 (PMID: 16914181)
10)Miura, Y., Sakurai, Y., Hayakawa, M., Shimada,
Y., Zempel, H., Sato, Y., Hisanaga, S., Endo, T. Translocation of lysosomal
cathepsin D caused by oxidative stress or proteasome inhibition in primary
cultured neurons and astrocytes. Biol Pharm Bull 33:22-28, 2010 (PMID:
20045930)
作成者
三浦ゆり、遠藤玉夫 20111130
Update 20120517