
|
 |
MGAT3; MANNOSYL (BETA-1,4-)-GLYCOPROTEIN
BETA-1,4-N-ACETYLGLUCOSAMINYLTRANSFERASE
[別名]
GNT-III;
N-acetylglucosaminyltransferase-III
キーワード
N結合型糖鎖、バイセクティングGlcNAc、がん
歴史とあらまし
1982年に酵素活性が報告され(Ref 1)、1992年に遺伝子がクローニングされた(Ref 2)。
分子構造
533アミノ酸からなるII型膜タンパク質である。Mn2+などの2価金属イオンが活性に必要である。単一エクソンにコードされている。
機能
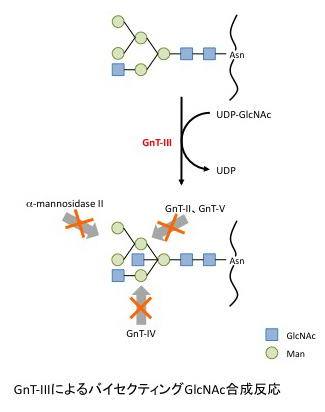
N結合型糖鎖の合成過程においてコアβマンノースにβ 1,4GlcNAc残基を付加してバイセクティングGlcNAcと呼ばれるユニークな糖鎖構造を形成する。バイセクティングGlcNAcの付加によりαマンノシダーゼII、GnT-II、IV、Vの反応が阻害され、複合型糖鎖の形成阻害や側鎖の伸長低下が起こる(Ref 3)。
老化・老年病における意義
N結合型糖鎖にGnT-Vによってβ 1,6GlcNAcが付加されると、がん細胞の転移能が増加する。逆にGnT-IIIを過剰発現させてGnT-Vの反応を阻害すると、がん細胞の転移が抑えられることが報告されている(Ref 4)。また、GnT-IIIを神経細胞で過剰発現させるとアルツハイマー病の原因とされるアミロイドβの産生が抑制されるという報告もある(Ref 5)。
Database
参考文献
1) Narasimhan S. Control of glycoprotein synthesis. UDP-GlcNAc:glycopeptide
beta 4-N-acetylglucosaminyltransferase III, an enzyme in hen oviduct which
adds GlcNAc in beta 1-4 linkage to the beta-linked mannose of the
trimannosyl core of N-glycosyl oligosaccharides. J. Biol. Chem.
257:10235-42, 1982 (PMID: 6213618)
2) Nishikawa A, Ihara Y, Hatakeyama
M, Kangawa K, Taniguchi N. Purification, cDNA cloning, and expression of
UDP-N-acetylglucosamine: beta-D-mannoside
beta-1,4N-acetylglucosaminyltransferase III from rat kidney. J. Biol. Chem.
267:18199-204, 1992 (PMID: 1325461)
3) Easton EW, Bolscher JG, van den
Eijnden DH. Enzymatic amplification involving glycosyltransferases forms the
basis for the increased size of asparagine-linked glycans at the surface of
NIH 3T3 cells expressing the N-ras proto-oncogene. J. Biol. Chem.
266:21674-80, 1991 (PMID: 1657976)
4) Yoshimura M, Nishikawa A, Ihara Y,
Taniguchi S, Taniguchi N. Suppression of lung metastasis of B16 mouse
melanoma by N-acetylglucosaminyltransferase III gene transfection. Proc.
Natl. Acad. Sci. U.S.A. 92:8754-8758, 1995 (PMID: 7568011)
5)
Akasaka-Manya K., Manya H., Sakurai Y., Wojczyk B.S., Kozutsumi Y., Saito
Y., Taniguchi N., Murayama S., Spitalnik S.L., Endo T. Protective effect of
N-glycan bisecting GlcNAc residues on beta-amyloid production in Alzheimer's
disease. Glycobiology 20:99-106, 2010 (PMID: 19776078)
作成者
赤阪(萬谷)啓子、遠藤玉夫 20111130
Update 20120628