
|
 |
POLG; POLYMERASE, DNA, GAMMA
[別名]
POLG1
POLG, CATALYTIC SUBUNIT
POLGA; POLG-ALPHA
キーワード
mtDNA, multiple deletions, depletion, somatic point mutations, PEO
歴史とあらまし
ヒトのミトコンドリアDNA (mtDNA)複製酵素DNAポリメラーゼ・ガンマ (POLG) は、現在までにミトコンドリアにおいて見つかっている唯一のDNAポリメラーゼである。2001年にmtDNA多重欠失を伴う常染色体優性遺伝性進行性外眼筋麻痺(AD-PEO)の家系がこの酵素の遺伝子変異が原因で発症することが初めて報告され(Ref.1)、それ以降、現在までに40種類弱の変異の報告がある(Ref.2-4)。一方、乳幼児期に発症し進行性の知能低下、難治性けいれん、小脳失調などを特徴とする神経変性疾患で肝障害を伴うAlpers症候群は、heterogeneousな疾患として知られており、長い間病因が不明であったが、その病因の一つがPOLG遺伝子変異であることがわかった(Ref.5)。興味深いことに、この疾患では患者のmtDNAコピー数が減少しdepletion(枯渇)が検出される。
分子構造
ヒトのmtDNAの複製酵素POLGは、POLG (POLG1)遺伝子にコードされた140 kDaのcatalytic subunit:p140と、POLG2遺伝子にコードされた55 kDaのaccessory subunit:p55によるヘテロダイマーとして存在する(Ref.6, 7)。
機能
POLGのcatalytic subunitにDNAポリメラーゼ活性と校正機能である3'→5' exonuclease活性がある。このcatalytic subunitをノックアウトしたマウスではmtDNAコピー数が著減(枯渇)し胎児致死性になる(Ref.8)。同じcatalytic subunitの3’→5’ proofreading exonuclease活性機能をコードする部分に点変異を導入し、校正機能に必要なアスパラギン酸残基をアラニン残基に置換したマウスでは、mtDNAの点変異頻度が増加し、mtDNA欠失、mtDNA depletion(枯渇)など多様なmtDNA異常が出現し蓄積することが明らかになった。その結果、呼吸鎖酵素活性が低下し、細胞の形態異常が認められ、体重減少、白髪化、脱毛、亀背、骨量の低下、骨格筋肉量の減少 (sarcopenia) などの老化現象が早期から観察され、極めて短寿命となった(Ref.9)。したがって、mtDNA変異が蓄積することにより、細胞へのエネルギー供給が低下し、細胞や組織を障害することで、結果的に老化を促進する可能性が示された。このマウスの組織では老化の原因の一つとされる活性酸素種(ROS)が増加しておらず、むしろ蛋白分解酵素caspase-3の活性化によるapoptosisプロセスの進行と、それに伴う細胞数減少が老化にとって重要である可能性が報告されている(Ref.10,11)。
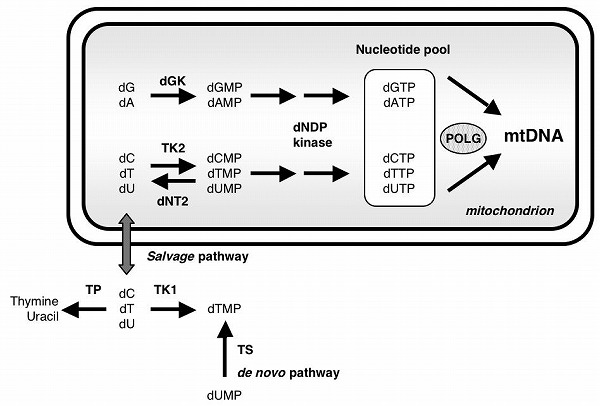
Mitochondrial nucleoside/nucleotide metabolism. dGK, deoxyguanosine kinase; TK,
thymidine kinase; dNT2, deoxynucleotidase 2; TP, thymidine phosphorylase; TS,
thymidine synthetase; dNDP, deoxynucleoside diphosphate; dG, deoxyguanosine;
dGMP, deoxyguanosine monophosphate; dGTP, deoxyguanosine triphosphate; dA,
deoxyadenosine; dAMP, deoxyadenosine monophosphate; dATP, deoxyadenosine
triphosphate; dC, deoxycytidine; dCMP, deoxycytidine monophosphate; dCTP,
deoxycytidine triphosphate; dT, deoxythymidine; dTMP, deoxythymidine
monophosphate; dTTP, deoxythymidine triphosphate; dU, deoxyuridine; dUMP,
deoxyuridine monophosphate; dUTP, deoxyuridine triphosphate. Modified from
Ref.12.
老化・老年病における意義
POLG遺伝子変異に伴うPEO症例においては、患者の年齢が高くなるに従って、特にmtDNA発現制御領域の変異蓄積が増大すると報告されており(Ref.13)、ヒトの加齢とmtDNA変異蓄積との密接な関連性を示唆する。体細胞のmtDNA変異の蓄積が老化における機能障害の重要な要素となることは、ROSの関与などで議論が分かれているが、POLG異常症や別項で紹介する上染色体劣性遺伝性のミトコンドリア病であるmitochondrial neurogastrointestinal encephalomyopathy (MNGIE)などに対する詳細な検討、POLG変異モデルを用いた研究によって、近年、目覚ましい進展がみられ、今後の研究の更なる発展が期待される。
Database
Mitochondrial DNA polymerase gamma
Human DNA Polymerase Gamma Mutation
Database
参考文献
1) Van Goethem G, Dermaut B, Lofgren A, Martin JJ, Van Broeckhoven C.
Mutation of POLG is associated with progressive external ophthalmoplegia
characterized by mtDNA deletions. Nat Genet 28:211-212, 2001 (PMID:
11431686)
2) Stuart GR, Santos JH, Strand MK, Van Houten B, Copeland WC.
Mitochondrial and nuclear DNA defects in Saccharomyces cerevisiae with
mutations in DNA polymerase gamma associated with progressive external
ophthalmoplegia. Hum Mol Genet 15:363-374, 2006 (PMID: 16368709)
3)
Filosto M, Mancuso M, Nishigaki Y, Pancrudo J, Harati Y, Gooch C, Mankodi A,
Bayne L, Bonilla E, Shanske S, Hirano M, DiMauro S. Clinical and genetic
heterogeneity in progressive external ophthalmoplegia due to mutations in
polymerase gamma. Arch Neurol 60:1279-1284, 2003 (PMID: 12975295)
4)
Copeland WC, Ponamarev MV, Nguyen D, Kunkel TA, Longley MJ. Mutations in DNA
polymerase gamma cause error prone DNA synthesis in human mitochondrial
disorders. Acta Biochim Pol 50:155-167, 2003 (PMID: 12673356)
5) Naviaux
RK, Nguyen KV. POLG mutations associated with Alpers' syndrome and
mitochondrial DNA depletion. Ann Neurol 55:706-712, 2004 (PMID: 15122711)
6) Copeland WC, Annu Rev Med 59, 131-146, 2008 (PMID: 17892433)
7) Milone
M, Benarroch EE, Wong LJ. POLG-related disorders: defects of the nuclear and
mitochondrial genome interaction. Neurology 77:1847-1852, 2011 (PMID:
22084276)
8) Hance N, Ekstrand MI, Trifunovic A. Mitochondrial DNA
polymerase gamma is essential for mammalian embryogenesis. Hum Mol Genet
14:1775-1783, 2005 (PMID: 15888483)
9) Trifunovic A, Wredenberg A,
Falkenberg M, Spelbrink JN, Rovio AT, Bruder CE, Bohlooly-Y M, Gidlof S,
Oldfors A, Wibom R, Tornell J, Jacobs HT, Larsson NG. Premature ageing in
mice expressing defective mitochondrial DNA polymerase. Nature 429:417-423,
2004 (PMID: 15164064)
10) Kujoth GC, Hiona A, Pugh TD, Someya S, Panzer
K, Wohlgemuth SE, Hofer T, Seo AY, Sullivan R, Jobling WA, Morrow JD, Van
Remmen H, Sedivy JM, Yamasoba T, Tanokura M, Weindruch R, Leeuwenburgh C,
Prolla TA. Mitochondrial DNA mutations, oxidative stress, and apoptosis in
mammalian aging. Science 309:481-484, 2005 (PMID: 16020738)
11)
Trifunovic A, Hansson A, Wredenberg A, Rovio AT, Dufour E, Khvorostov I,
Spelbrink JN, Wibom R, Jacobs HT, Larsson NG. From the Cover: Somatic mtDNA
mutations cause aging phenotypes without affecting reactive oxygen species
production. Proc Natl Acad Sci USA 102:17993-17998, 2005 (PMID: 16332961)
12) Hirano M, Marti R, Spinazzola A, Nishino I, Nishigaki Y. Thymidine
phosphorylase deficiency causes MNGIE: an autosomal recessive mitochondrial
disorder. Nucleosides Nucleotides Nucleic Acids 23:1217-1225, 2004 (PMID:
15571233)
13) Wanrooij S, Luoma P, van Goethem G, van Broeckhoven C,
Suomalainen A, Spelbrink JN. Twinkle and POLG defects enhance age-dependent
accumulation of mutations in the control region of mtDNA. Nucleic Acids Res
32:3053-3064, 2004 (PMID: 15181170)
作成者
西垣 裕 20111225
Update 20120228