
|
 |
CALM1; CALMODULIN 1
[別名]
PHOSPHORYLASE KINASE, DELTA SUBUNIT; PHKD
CALMODULIN 2; CALM2
[別名]
PHKD2
CALM3; CALMODULIN 3
[別名]
PHKD3
キーワード
カルシウム、カルシウム-カルモジュリン複合体、シグナル伝達
歴史とあらまし
CALcium MODULated proteINから名付けられた、真核細胞に広く存在するカルシウム結合タンパク質。cAMP-ホスホジエステラーゼの活性化因子として1970年に発見された。その後、アデニル酸シクラーゼ、赤血球膜Ca2+-Mg2+-ATPアーゼ、NAD+-キナーゼなどもカルシウムイオンの存在下で活性化することが明らかにされた。
分子構造
カルモジュリンの構造は、よく保存されている。ヒトのカルモジュリンは全体で149アミノ酸からなり、アセチル化、メチル化、リン酸化、ユビキチン化をはじめとして様々な翻訳後修飾を受ける。4つのEF-handを持ち、カルシウム結合部位が4箇所ある。カルシウムの結合定数は106程度で、カルモジュリン1分子につき2分子のカルシウムが結合する。カルシウムの結合により構造変化を引き起こし、特定のタンパク質と相互作用する。
機能
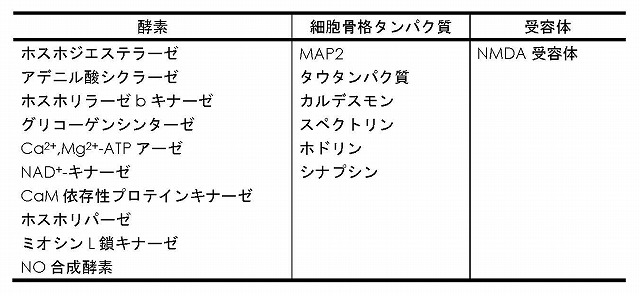
カルシウムに結合し、カルシウム-カルモジュリン複合体を作って様々なタンパク質の機能制御を行う。カルシウムイオンを介したシグナル伝達、筋収縮、細胞分裂、神経伝達などに関与している。カルシウム-カルモジュリン複合体は、多くの酵素と結合しその酵素を活性化する。また、細胞骨格タンパク質と結合することにより、細胞骨格機能制御を行う。主なカルモジュリン結合タンパク質を表に示す。
老化・老年病における意義
1987年McLachlanらにより、カルモジュリンの発現がアルツハイマー脳において低下することが報告された(Ref.
1)。さらに、アルツハイマー脳から抽出したカルモジュリンは、ホスホジエステラーゼを活性化する能力が低下していることも明らかにされており(Ref.
1)、アルツハイマー脳ではカルモジュリンの量と質の両面における低下により、カルシウムホメオスタシスの変動をきたしていると考えられる。
自然老化においても、カルモジュリンの機能低下が報告されている。Squierらは1996年、老齢ラット脳において、カルモジュリンのCa2+-ATPアーゼ活性化能が低下していることを明らかにした(Ref.
2)。彼らは、メチオニンの酸化がカルモジュリンのCa2+-ATPアーゼ活性化能低下の原因であると報告している(Ref. 3,
4)。またNMRを用いた研究により、メチオニンの酸化がカルモジュリンの立体構造に変化をもたらし、Ca2+-ATPアーゼとの相互作用に影響を及ぼすことも明らかにされた(Ref.
5)。さらにTodaらは、二次元電気泳動によるプロテオミクス解析により、老齢マウス海馬においてカルモジュリンの発現が低下することを報告している(Ref.
6)。また、MSデータの詳細な解析から、カルモジュリンのEF-hand 4でのメチオニンの酸化(Met 144及びMet
145のスルホキシド化)が加齢により増加することを明らかにした(Ref. 5)。メチオニンの酸化は、カルモジュリンの安定性を低下させ(Ref.
7)、プロテアソームにより分解されやすくすることが報告されており(Ref.
8)、老化によるカルモジュリン発現量の低下はメチオニンの酸化が影響していると考えられる。
Database
参考文献
1. McLachlan DR, Wong L, Bergeron C, Baimbridge KG, Calmodulin and calbindin
D28K in Alzheimer disease. Alzheimer Dis Assoc Disord. 1987; 1(3): 171-9. (PMID:
2840101)
2. Michaelis ML, Bigelow DJ, Schöneich C, Williams TD,
Ramonda L, Yin D, Hühmer AF, Yao Y, Gao J, Squier TC. Decreased plasma
membrane calcium transport activity in aging brain. Life Sci. 1996; 59(5-6):
405-12. (PMID: 8761328)
3. Yao Y, Yin D, Jas GS, Kuczer K, Williams TD, Schöneich C, Squier TC.
Oxidative modification of a carboxyl-terminal vicinal methionine in
calmodulin by hydrogen peroxide inhibits calmodulin-dependent activation of
the plasma membrane Ca-ATPase. Biochemistry. 1996; 35(8): 2767-87. (PMID:
8611584)
4. Gao J, Yin D, Yao Y, Williams TD, Squier TC. Progressive
decline in the ability of calmodulin isolated from aged brain to activate
the plasma membrane Ca-ATPase. Biochemistry. 1998; 37(26): 9536-48. (PMID:
9649337)
5. Anbanandam A, Bieber Urbauer RJ, Bartlett RK, Smallwood
HS, Squier TC, Urbauer JL. Mediating molecular recognition by methionine
oxidation: conformational switching by oxidation of methionine in the
carboxyl-terminal domain of calmodulin. Biochemistry. 2005; 44(27): 9486-96.
(PMID: 15996103)
6. Toda T, Nakamura M, Morisawa H, Hirota M, Nishigaki R, Yoshimi Y.
Proteomic approaches to oxidative protein modifications implicated in the
mechanism of aging. Geriatr Gerontol Int. 2010; 10 Suppl 1: S25-31. (PMID:
20590839)
7. Gao J, Yin DH, Yao Y, Sun H, Qin Z, Schoneich C,
Williams TD, Squier TC. Loss of conformational stability in calmodulin upon
methionine oxidation. Biophys J. 1998; 74(3): 1115-34. (PMID:
9512014)
8. Strosova M, Voss P, Engels M, Horakova L, Grune T.
Limited degradation of oxidized calmodulin by proteasome: formation of
peptides. Arch Biochem Biophys. 2008; 475(1): 50-4. (PMID:
18455497)
作成者
三浦ゆり、戸田年総 20121120
Update 20121120